https://www.nature.com/articles/s41556-024-01565-x
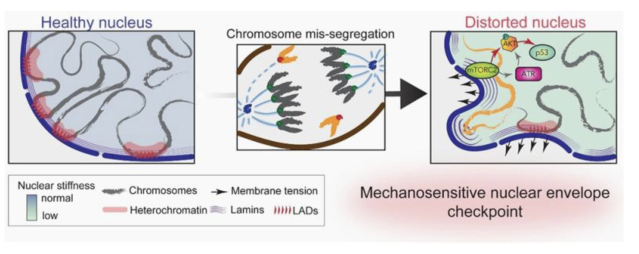
Incorrect chromosome segregation during cell division leads to abnormalities that disrupt cell function. Cells with abnormal chromosome numbers consequently activate mechanisms to prevent their propagation. A study reveals how these chromosomal abnormalities are detected. These results highlight a novel role for the mechanics of the nucleus in this process. Aneuploidy, a condition in which cells have an incorrect number of chromosomes, is observed in 90% of solid tumors. It results from errors in the segregation of chromosomes from the mother cell to the two daughter cells during mitosis and leads to the activation of p53, a key protein that prevents abnormal cells from dividing. When p53 is mutated, which occurs, on average in one in two cancers, theses cells can continue to divide, accumulate more mutations and, ultimately, lead to the development of cancer. A mechanoreceptive nuclear checkpoint causes cell cycle arrest after chromosome mis-segregation. Errors in chromosome segregation during mitosis lead to deformation and softening of the nucleus, reduced levels of heterochromain at the nuclear periphery and defects in laminate assembly. These alterations increase tension on the nuclear envelope of daughter cells, leading to activation of mTORC2 and ATR mechanoreceptors, triggering cell arrest in a p53 manner. 01/25
https://www.eurostemcell.org/fr/video-diabetes-and-stem-cells
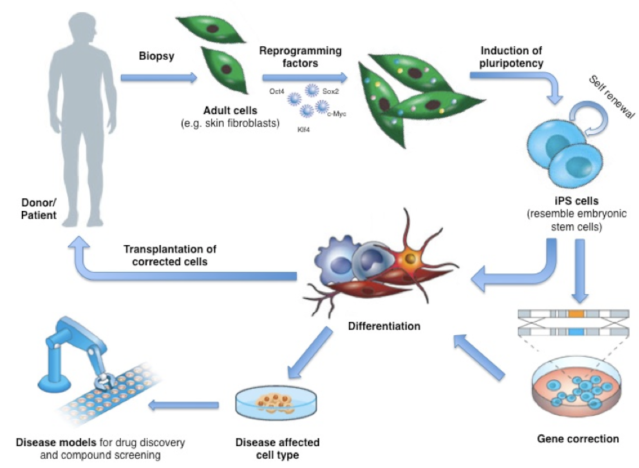
Une nouvelle technique de greffe autologue, basée sur des cellules souches reprogrammées IPS en cellules pancréatiques, a permis de guérir une patiente atteinte de diabète de type 1. Le diabète de type 1 est une maladie autoimmune où les cellules pancréatiques permettant la production d'insuline pour la régulation de la glycémie sont détruites. Cette patiente n'a plus besoin d'injections d'insuline grâce à ces IPS reprogrammées en cellules pancréatiques. 10/24
https://www.nature.com/articles/s41586-023-06802-1
https://www.altoslabs.com/science
https://www.inserm.fr/dossier/cellules-souches-pluripotentes-induites-ips/#
Prédire l'âge de nos organes avec une prise de sang. Avec le temps, nos cellules se renouvellent moins voire plus du tout, c'est la sénescence. Par exemple, la peau produit de moins en moins de collagène (fibroblastes) et perd donc son élasticité ce qui provoque des rides. Des scientifiques ont prélevé un simple échantillon de sang chez plus de 5000 volontaires, et ont regardé la présence de milliers de protéines. En fonction de leur quantité, ils ont déduit l'activité de certains organes comme le foie, le rein, les poumons... Avec un algorithme, ils ont prédit l'âge physiologique, biologique soit un âge des organes et l'ont comparé avec l'âge chronologique. Résultat: les organes viellissent à un rythme différent. Le vieillissement est la déterioration physiologique de nos organes. Avec 3 milliards de fonds d'investissement, Altos Labs est la start-up biomédicale la plus riche de toutes. Son objectif est de restaurer la "jeunesse" des cellules et inverser leur vieillissement ceci en déprogrammant les cellules différenciées. 12/23
La géroscience est en marche! Les marqueurs de la vieillesse sont: sénescence des cellules (cellules comme "zombie" mais qui produisent des molécules toxiques pour les cellules environnantes), peu ou pas de renouvellement cellulaire, endommagement du génome, diminution de la communication intercellulaire, dysfonctionnement mitochondrial, dysbiose du microbiote, inflammation chronique et racourcissement des télomères. Altos Lab et de nombreux autres laboratoires travaillent sur la déprogrammation de notre génome soit de nos 220 types cellulaires afin de convertir des cellules différenciées adultes en cellules souches pluripotentes induites IPS (Induced Pluripotent Stem cells/ Nobel Prize 2012) soit des cellules immatures capables de redonner n'importe quel type de cellules de l'organisme et ceci à l'infini (mêmes propriétés que les cellules souches embryonnaires). La reprogrammation de cellules différenciées en cellules IPS consiste à les modifier génétiquement pour réactiver des gènes et des signaux embryonnaires de dédifférenciation et de prolifération illimitée, caractéristiques d'une cellule souche pluripotente. Réactiver la pluripotence éteint les gènes de différenciation exprimés par la cellule au stade adulte. La "réexpression de " de 4 gènes soit des facteurs de transcription OKMS, surexprimés dans les cellules souches embryonnaires, est suffisante et nécessaire pour reprogrammer une cellule adulte. Il y a donc suppression de deux propriétés épigénétiques: différenciation et âge de la cellule. Ces IPS donnent de grans espoirs pour de nombreuses maladies telles que Parkinson, cancers. De même, si tous les types cellulaires d'un animal sont reprogrammées, l'animal gagne 15 à 20% de vie en bonne santé! Autre cible: les télomères des chromosomes. Les télomères sont des séquences répétées d'ADN situées à l'extrêmité des chromosomes. A chaque division cellulaire, les télomères racourcissent ce qui mène après de nombreuses division à un racourcissement trop important des telomères et un arrêt définitif de la division. la cellule devient sénescente. Ainsi, modifier génétiquement les cellules en bloquant l'enzyme la télomérase serait une autre solution pour ralentir le vieillissement. D'autres options sont aussi testées. A suivre.
Découverte d'un génome qui ne ressemble à aucun autre. En 1977, est découverte un type de bactériophage (virus qui infecte les bactéries) utilisant un alphabet génétique tout à fait unique: l'adénine est remplacée par de la diaminopurine appelée Z. L'alphabet génétique de ce virus n'est donc pas ATGC mais ZTGC. Ce génome a été baptisé génome Z. Des études montrent que ce génome est beaucoup plus répandu qu'on ne le pensait. Ce nucléotide Z donnerait des avantages au virus: l'ADN-Z serait plus stable à des températures élevées et résisterait mieux à certaines protéines présentes dans les bactéries que le virus infecte. De plus, ce génome Z est présent dans plus de 200 types de bactériophages. L'origine exacte de ce génome est pour le moment inconnue. 04/21
https://science.sciencemag.org/content/372/6541/520
https://www.youtube.com/watch?v=39TMmUs_9JI
Selon une étude, les enfants des survivants de la catastrophe de Tchernobyl ne portent pas de mutations génétiques supplémentaires. Lors de l'explosion de la centrale nucléaire, le 26 avril 1986, l'accident de Tchernobyl, a exposé des millions de personnes à des contaminants radioactifs. Ces rayonnements ionisants sont très cancérigènes. Par contre, les conséquences sur les mutations génétiques hérédiataires n'étaient pas encore connues. Une équipe internationale a séquencé les génomes de 130 enfants et de leurs parents. Ces enfants sont nés entre 1987 et 2002 et de parents qui ont été très exposés aux radiations. Les scientifiques ont voulu savoir si les enfants étaient nés avec plus de mutations de novo, c'est à dire, une mutation de l'ADN qui survient dans les gamètes d'un des deux parents. Contrairement à ce qui était attendu, les enfants des survivants de Tchernobyl ne portent pas plus de mutations que dans la population générale. L'exposition aurait eu un impact minime sur la santé des générations suivantes. Ces résultats pourraient être rassurants pour les personnes qui vivaient à Fukushima où les doses de rayonnement ont été moins fortes que celles de Tchernobyl. 04/21.
https://science.sciencemag.org/content/early/2021/04/21/science.abg2365
https://nextstrain.org/ncov/global/2020-05-14
Dans une étude parue dans Nature Communications, une équipe du CNRS a découvert le point faible du SARS-CoV2: son ARN polymérase. La polymérase est une enzyme qui est codée par le génome du virus et qui est chargée de faire une copie fidèle de son matériel génétique: dans le cas du Coronavirus, il s'agit d'une longue molécule d'ARN. Parfois, il y a des erreurs, mais cette polymérase est capable de réparer les erreurs qu'elle fait pour assurer une stabilité génétique. Ces chercheurs ont mis en évidence que pour le SARS-CoV 2, cette polymérase est extrêmement rapide. Elle est 10 fois plus rapide que chez le virus de l'hépatite C par exemple, alors que la molécule d'ARN du Coronavirus est 3 fois plus longue. L'avantage pour le virus, c'est que cela laisse moins de temps au système immunitaire pour le détecter. Mais cet atout est aussi une faiblesse pour le Coronavirus. Le fait que cette copie soit plus rapide, cela se fait au détriment de la fidélité de la réplication, et donc entraine beaucoup de mutations. Des médicaments avec des molécules, qui s'insèreraient lors de cette rapide réplication et ainsi entraineraient des mutations létales pour le virus, constituent un espoir de lutte contre le Coronavirus. Oct/20